Главная→ Информация для покупателей→ Новости науки→ Молекулярные маяки сигнализирует о тканевой гипоксии посредством ультразвука
Молекулярные маяки сигнализирует о тканевой гипоксии посредством ультразвука
Области гипоксии (низкого уровня кислорода в тканях) являются признаками быстрорастущих раковых образований или закупорки, сужения кровеносных сосудов, встречающихся, например, при инсульте или болезнях периферических артерий. Ученые из Университета штата Иллинойс нашли новый неинвазийный способ поиска гипоксических пятен в тканях в режиме реального времени.
Исследователи разработали кислород-чувствительный молекулярный маяк, который испускает ультразвуковые сигналы в ответ на свет, процесс, называемый фотоакустической визуализацией.
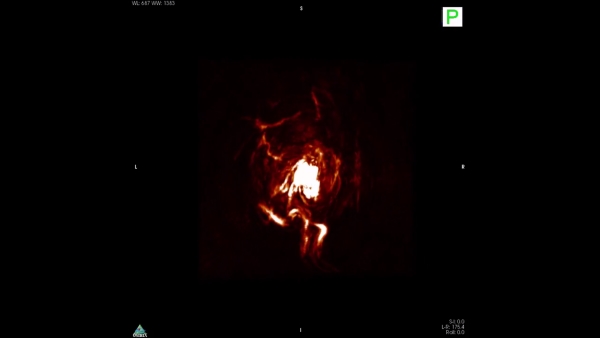
Трехмерная визуализация гипоксической опухоли.
Это не инвазивный, более точный и менее дорогостоящий метод, чем применяющиеся сейчас в клинике радио-изотопное сканирование и позитронно-эмиссионная томография. В статье, опубликованной в Nature Communications, исследователи продемонстрировали способность пробного образца визуализировать гипоксические опухоли и суженные артерии у мышей.
«Метод мог бы дать врачу трехмерное изображение в реальном времени, что помогло бы проводить как хирургическое, так и консервативное лечение», — сказал руководитель исследования профессор химии Джефферсон Чан. В соавторстве с ним выступили аспирант Хейли Нокс и профессор биоинженерии Лоренсе Добруский.
«Способность обнаруживать заболевания без инвазивных методов вмешательства и в то же время не полагаться только на косвенные методы, действительно бесценна. Наш метод не только визуализирует гипоксию, но и устанавливает стадию ее развития», — сказал Чан.
Современные методы обнаружения гипоксии в ткани могут идентифицировать только хроническую гипоксию и, следовательно, не могут помочь врачам найти раковые образования на начальных стадиях или острые состояния, требующих немедленного вмешательства, такие, например, как инсульт, добавил Чан. Доступные сейчас методы является либо инвазивными процедурами, связанными с введением крупных электродных игл или косвенной визуализацией с помощью радиоактивных зондов, что имеет дополнительные проблемы, связанные с нецелевой активацией и помехами.
Молекулярные зонды, разработанные группой Чан, активизируются при развитии дефицита кислорода. При возбуждении светом они продуцируют ультразвуковой сигнал, позволяющий получить прямое трехмерное изображение областей гипоксии. Ученые протестировали систему на клеточных культурах, а затем на живых мышах с раком молочной железы и мышах с суженными артериями на ногах.

Аспирант Хейли Нокс и профессор химии Джефферсон Чан, разработавшие фотоакустический молекулярный зонд.
«Система, которую мы использовали в этом исследовании, является доклинической и предназначена для опытов на животных. Для адаптации метода в клинических условиях достаточно использовать простейшее оборудование медицинского назначения — обычный ультразвуковой аппарат и оснастить его источником света — вы можете купить светодиоды примерно за 200 долларов, которые достаточно сильны и безопасны для клинического использования», — сказал Чан. Врачи смогут вводить фотоакустические молекулы пациенту либо путем инъекции в вену, либо непосредственно в участок опухоли, а затем использовать модифицированную ультразвуковой аппарат для визуализации интересующей области.
Исследователи обнаружили, что их фотоакустический метод может обнаружить гипоксию через несколько минут после того, как артерия мыши была сжата, что дает новые возможности в диагностике, например, это позволит быстро найти очаг инсульта или сгусток крови в глубоких тканях. У мышей с раком зонды позволили провести детальное трехмерное ультразвуковое исследование гипоксических опухолей.
«Мы знаем, что много опухолей являются гипоксическими, поэтому были разработаны новые противораковые препараты, активирующихся в условиях дефицита кислорода. Но в клинических испытаниях они были неэффективны, поскольку не все опухоли являются гипоксическими», — сказал Чан. «Фотоакустическая визуализация даст ученым и врачам возможность неинвазивно заглянуть внутрь опухолей и определить, является ли опухоль пациента гипоксичной, а значит, поможет решить, подойдет ли для лечения новый препарат. Если опухоль не выглядит гипоксичной, то нужен другой тип лечения.»
Исследователи заявили, что еще одним преимуществом является низкая стоимость производства молекул и их длительный срок хранения. Они могут оставаться стабильными в течение многих лет, тогда как радиоактивные молекулы должны использоваться вскоре после изготовления и требуют специальной подготовки для использования.
Чан и его коллеги исследуют также другие типы фотоакустических молекул, которые могут визуализировать и другие процессы. Например, они работают над зондами, которые могут обнаруживать определенные виды рака, чтобы можно было найти места в теле пациента, куда метастазировала раковая опухоль.
«Теперь можно не только обнаружить раковую опухоль и описать ее свойства, но и расширить возможности для повышения качества ухода за пациентами. Наконец-то мы можем видеть весь айсберг, а не его верхушку», — сказал Чан.
- 27 июля 2022
-
Вирус гепатита Е поражает эндотелиальные клетки микрососудов головного мозга
Ученые обнаружили, что как квазиоболочечные, так и необолочечные HEV могут аналогичным образом проникать через гематоэнцефалический барьер.
- 23 июля 2022
-
Усы как гидродинамические датчики добычи у кормящихся тюленей
Недавно ученые отметили замечательный случай, когда усы способствовали добыванию пищи млекопитающими в экстремальных подводных условиях: глубоком, темном океане.
- 20 июля 2022
-
Функциональная ближняя инфракрасная спектроскопия выявляет активность мозга в движении
Метод fNIRS продвинулся от относительно простых измерений изменений содержания кислорода в крови к сложному методу регистрации реакций мозга в реальном времени, связанных с широким спектром действий и когнитивных задач.
- 16 июля 2022
-
Инъекция шванномы с ослабленным штаммом сальмонеллы индуцирует противоопухолевый иммунитет
Поскольку бактериальная иммунотерапия использовалась при лечении некоторых злокачественных новообразований, ученые оценили ослабленный штамм сальмонеллы в качестве иммунотерапии доброкачественной мышиной шванномы.
- 13 июля 2022
-
Изучен высоко обратимый металлический цинковый анод
Перезаряжаемая металлическая цинковая батарея на сегодняшний день считается важной технологией, которая может устранить цепочку поставок и экономический кризис, вызванный химией на основе лития.






