Возможна ли универсальная защита от всех штаммов гриппа
В США сейчас эпидемия вируса гриппа. В настоящее время он распространен в 49 штатах и Пуэрто-Рико, с октября им переболело тысячи людей, как сообщают Центры по контролю и профилактике заболеваний. Каждый год в мире из-за гриппа умирает десятки тысяч человек.
«Сейчас создание универсальной вакцины против гриппа должно стать более приоритетным делом, чем когда бы то ни было», — говорит Энтони Фаучи, директор Национального института аллергии и инфекционных заболеваний (NIAID).
Ученые уже давно ищут вакцину против гриппа, которая защищала бы людей от сезона до сезона только одной прививкой, как это свойственно вакцинам против кори или ветряной иммунной системы организма, поэтому новая вакцина против гриппа должна разрабатываться каждый год или через год.
Вирус гриппа выглядит как шарик с растущими из него «грибами». «Грибы» — поверхностные белки: гемагглютинин и нейраминидаза. Гемагглютинин помогает вирусу связываться с клетками-хозяевами, чтобы заразить их, тогда как нейраминидаза помогает в распространении вируса после его репликации в клетке-хозяине.
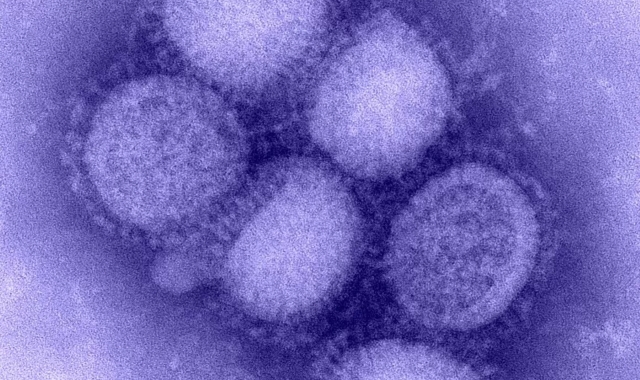
Микрофотография вируса H1N1
Для создания эффективной вакцины против гриппа главной мишенью всегда был гемагглютинин. Если вакцина сможет помешать гемагглютинину прикрепляться к инфицируемым клеткам и заражать клетки-хозяев, то это остановит вирус в самом начале его пути, говорит Тед Росс, микробиолог из Университета Джорджии в Афинах. Однако это довольно сложно, потому что «грибная головка» гемагглютинина быстро мутирует, поэтому антитела против одного типа такой головки не будут работать против мутантных версий.
Учитывая этот факт, Росс и его коллеги разработали способ прогнозировать эволюцию вируса, базируясь на прошлых последовательностях развития головок гемагглютинина определенного штамма гриппа. Исследователи создали смешанную молекулу гемагглютининовой головки для штамма гриппа H1N1 и использовали ее для разработки вакцины для иммунизации мышей. Вакцина защищала животных и от тех версий штамма, воздействию которых мыши никогда не подвергались прежде. В декабре 2017 года команда сообщила о подобных результатах для H3N2, штамма, который отвечает за особенно агрессивный сезон гриппа в этом году. Росс говорит, что вакцина, созданная с использованием этого вычислительного подхода, сейчас разрабатывается компанией Sanofi Pasteur и может пройти клинические испытания уже в 2019 году.
Ученые также изучают основание, на котором фиксируется гемагглютинин (образно выражаясь «ножку гриба»), так как это образование важно для того, чтобы вирус мог внедрить свой геном в клетку-хозяина. «Это то, что инициирует инфекцию», — говорит Флориан Краммер, микробиолог Медицинской школы Icahn на Mt. Синай в Нью-Йорке. Чтобы заразить клетку, «ножка гриба» гемагглютинина полностью перестраивается. «Это машина, — объясняет Краммер. «Она плохо переносит мутации, и если вы инициируете мутацию, то тем самым уничтожаете машину репликации, так как вирус не любит ее менять ».
Поскольку «ножка», на которой сидит гемагглютинин не любит изменений, это делает ее хорошей мишенью для вакцинации. Однако иммунная система, к сожалению, мало чувствительна к этой части белка. Краммер и его коллеги разработали молекулу гемагглютинина с головкой из различных штаммов гриппа, которые не циркулируют у людей и «ножку» из штамма, такого как H1N1. В сентябре 2017 исследователи сообщили года в Vaccines о создании ими вакцины с консервативной «ножкой», но вариабельными головками, активирующими антитела. Исследование проводилось на хорьках.
Другие команды испытывают в качестве потенциальных вакцин безголовые «ножки», созданные путем закрепления на «ножках» наночастиц ферритинового белка или путем создания генетических мутаций. Некоторые из этих методов сейчас переходят в клинические испытания, говорит Фаучи.
Он отмечает, что нейраминидаза была «забытым нелюбимым детищем» в процессе поиска более эффективной вакцины против гриппа, но сейчас ученые начинают разрабатывать и это направление исследований.
Создание антител против гемагглютинина и нейраминидазы может быть не единственным способом сделать оптимальную вакцину против гриппа. Принципиально другим подходом может стать усиление визуализации вируса для иммунной системы, нацеливание на него системы интерферонов организма. Белки интерферона I типа из клеток, таких как лейкоциты и фибробласты, являются одними из первых, кто реагирует, когда клетка инфицируется вирусом. Вирусу гриппа, однако, удается скрываться избегать обнаружения этими белками, благодаря наличию специальной защиты.
В исследовании, опубликованном 19 января в Science, вирусолог Рен Сан из Калифорнийского университете в Лос-Анджелесе, и его коллеги определили восемь генетических мутаций, которые делают вирус гриппа чувствительным к интерферонам клетки-хозяина. Затем они объединили мутантные штаммы в один вирус, создав живую ослабленную версию гриппа — аттенуированной вакцины, которая могла бы стимулировать реакцию иммунной системы, но не реплицировалась. Мыши, получившие вакцину, выжили, получая стандартную смертельную дозу различных штаммов гриппа, в то время как большинство мышей, которые не были иммунизированы, умерли. Этот подход может сделать вакцину против гриппа более эффективной, говорит Сан в своей статье в Science.
«Это по-настоящему ловкий маневр», — говорит биолог, изучающий Т-клетки Джон Тейяро из Научно-исследовательского института Скриппса в Ла-Холле, Калифорния. «Команда смогла мутировать этот вирус для повышения чувствительности интерферона без изменения иммунного ответа, что всегда является проблемой».
Этот подход может стать важным шагом на пути к оптимальной вакцине против гриппа, поскольку он безопасен и, как было показано, обеспечивает защиту сразу от нескольких штаммов гриппа. По словам Тейяро, эту технику можно комбинировать с теми, которые направлены на разработку антител против головок гемагглютинина для создания более совершенной вакцины против гриппа.
Энтони Фаучи говорит, что не достаточно создать универсальную вакцину против гриппа, нужно понять, как последовательное воздействие вируса и вакцинация влияет на иммунную систему. «Люди подвергаются воздействию гриппа на протяжении всей своей жизни», — говорит он. Каждый раз, когда человек сталкивается с этим вирусом, он может по-другому реагирует на будущие инфекции. Например, лица, родившиеся до 1918 года (год смертельной «испанской» пандемии гриппа, вызванной штаммом H1N1), легче переносили последующие заражения вирусом гриппа, чем те, которые родились позже и не сталкивались с данной инфекцией. То же самое относится к людям, родившимся до или после других опасных сезонов гриппа, таких как 1957, 1968 и 2009 годы.
«Это то, что мы называем иммунологическим импринтингом. Это противоречиво, но нам нужно знать, каково его влияние на создание широкоэффективной вакцины против гриппа », - говорит Фаучи.
Сейчас данная идея нашла свое применение в опытах. Например, Краммер и его коллеги эмулировали наличие иммунитета у взрослых людей к гриппу путем активации иммунной системы хорьков с помощью одной из форм вируса перед тестированием новой вакцины, разработанной к другой форме. «Грунтовка» в виде предварительной активации иммунной системы и вакцина оказались более эффективным способом предотвращения заражение, чем моновакцинация.
Понимание влияния ранее существовавшего иммунитета на эволюцию вируса также играет большую роль, особенно, учитывая, что сама вакцинация может влиять на эволюцию штаммов гриппа, отмечает Fauci и коллеги в статье, опубликованной летом прошлого года в Immunity. В статье описывается путь к созданию универсальной вакцины против гриппа. «Я вижу, что ведущаяся в данном направлении работа попадает в три корзины», — говорит Фаучи. «Есть корзина на развитие антител, корзина на усиление иммунного ответа на грипп и, наконец, корзина на предыдущее воздействие вируса и то, как это влияет на иммунную систему», — говорит он.